|
|
 当大部门医药行业的眼光停在PD-1类肿瘤药崎岖的出海之路时,有国产PD-1的国内上市申请被羁系部分拒绝。
当大部门医药行业的眼光停在PD-1类肿瘤药崎岖的出海之路时,有国产PD-1的国内上市申请被羁系部分拒绝。
6月12日早间,嘉和生物(6998.HK)在港交所公告称,已获国家药品监视管理局告知,杰诺单抗(GB226)用于治疗复发╱难治性外周T细胞淋巴瘤(PTCL)的新药上市申请未获答应。
这个消息并不忽然,此前,国家药监局政务服务流派官网公布的《2023年06月09日药品关照件待领取信息发布》中,嘉和生物的PD-1产物杰诺单抗注射液就在此中。由于药品答应文号一栏为“无”,业内有分析以为,该药的上市申请未得到答应。现在,公告确认了这一推测。从公开报道来看,这是初次在国内被拒批的国产PD-1。
嘉和生物建立于2007年,此次被拒的PD-1产物早在2020年7月尾被纳入优先审评名单,彼时嘉和生物表现,该药是现在首个在中国境内以致环球申请PTCL顺应证的PD-1单抗。
进入审评流程已经近三年,为何终极被拒?6月12日上午,嘉和生物方面向汹涌消息记者表现,外周T细胞淋巴瘤包罗有凌驾20种亚型,各亚型发病机制非常复杂,部门亚型发病机制尚不明白。现在环球没有PD-1产物被答应用于PTCL的治疗,以是国家药监局药审中央(CDE)对于相干顺应证产物的审评就更为审慎。
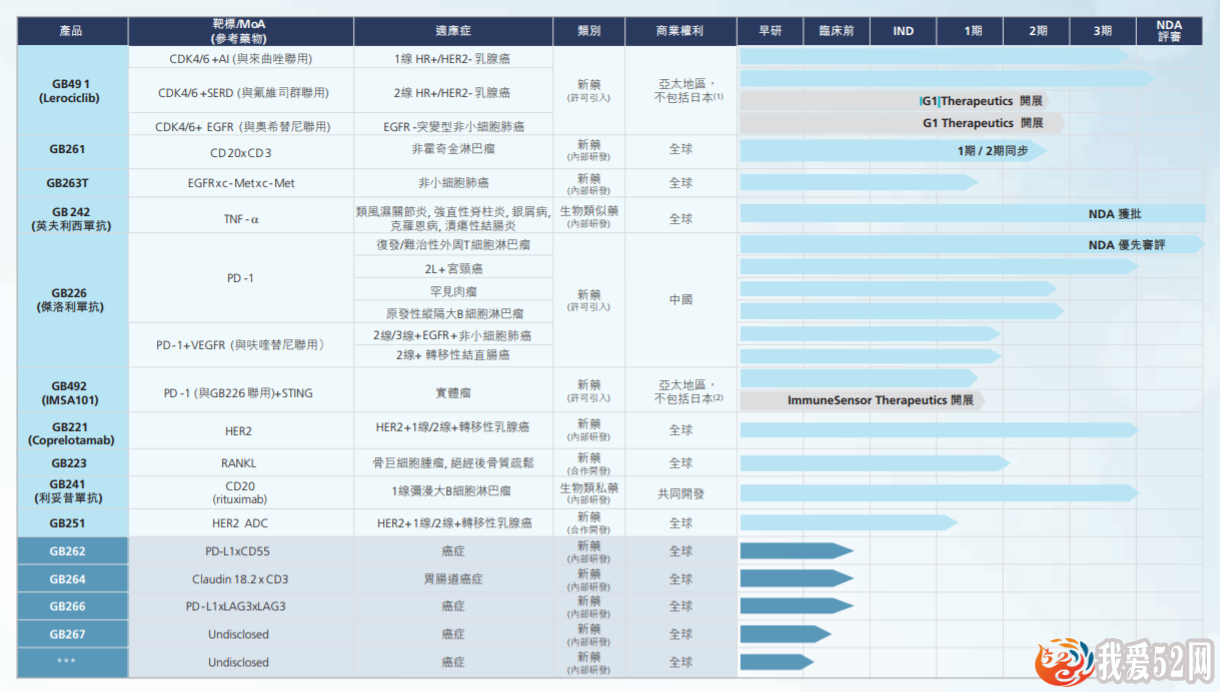 嘉和生物管线 泉源:2022年财报
嘉和生物管线 泉源:2022年财报
此次被拒对公司的影响,嘉和生物在港交所公告中夸大,公司预计其他临床试验或公司其他候选药物的开辟希望将不会受到影响。嘉和生物方面也向记者夸大,这款PD-1早已不是公司的焦点产物,从2022年开始,嘉和的焦点产物就变化为GB491(CDK4/6)、GB261(CD3/CD20)和GB263T(EGFR/cMET/cMET)三个双多抗产物,这三个焦点产物希望非常顺遂,后续也会继承快速推进。
PD-1是肿瘤相干的热门靶点,嘉和生物PD-1被纳入优先审评之时,国内PD-1竞争格局已初现“内卷”。2020年,除了K药、O药等入口PD-1,国产PD-1来自君实生物、信达生物、百济神州、恒瑞医药4家药企,颠末当年的医保会商,四家PD-1均进入国家医保目次。今后,随着获批数目增长以及各家产物代价的下调,PD-1也成为医药行业的“内卷之王”。
头豹研究院本年2月份公布的《2022年中国PD-(L)1克制剂赛道概览》指出,从2018年至今,中国市场已经有9款PD-1,4款PD-L1以及1款国产PD-1双抗获批上市,现在仍有2000多项临床试验举行中。此次嘉和生物PD-1被拒,无疑给这些仍在推进PD-1的创新药企发出了提示。
PD-1赛道扎堆的环境下,企业怎样制胜?上述概览陈诉指出,PD-(L)1赛道竞争猛烈,因此通过拓展顺应证范围、联适用药、以临床需求为导向等方式拓宽受益患者人群,同时企业也要提拔贸易化本领增长自身竞争本领。
停止发稿,嘉和生物跌1.11%,报1.78港元。 |
|